Lý do khiến hội đồng chưa đồng ý cấp phép đối với vắc-xin Nano Covax
Hội đồng chuyên môn của Bộ Y tế hiện chưa thông qua việc cấp phép khẩn cấp đối với vắc-xin Nano Covax, đồng thời đề nghị nhóm nghiên cứu bổ sung thêm dữ liệu về tính an toàn, miễn dịch và hiệu quả bảo vệ.
Theo đó, trong thời gian từ 8 giờ đến 15 giờ, ngày 29-8, Hội đồng tư vấn cấp giấy đăng ký lưu hành thuốc, nguyên liệu làm thuốc cùng với Lãnh đạo các Vụ, Cục liên quan (Vụ Pháp chế, Cục Khoa học Công nghệ và Đào tạo, Cục Y tế dự phòng) và đại diện Hội đồng Đạo đức trong nghiên cứu y sinh học Quốc gia, các chuyên gia thẩm định thuộc các Tiểu ban (Tiểu ban Pháp chế, Tiểu ban Chất lượng thuộc Viện Kiểm định Quốc gia vắc-xin và sinh phẩm y tế (NICVB), Tiểu ban Dược lý, Lâm sàng thuộc Trung tâm Dược lý lâm sàng – Trường Đại học Y Hà Nội) đã họp xem xét hồ sơ đề nghị cấp giấy đăng ký lưu hành vắc-xin Nano Covax do Công ty cổ phần công nghệ sinh học dược Nanogen đăng ký và sản xuất.
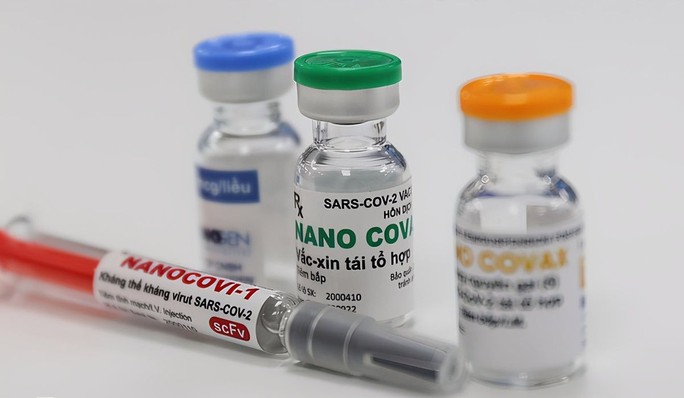
Vắc-xin Nano Covax ngừa Covid-19 do Việt Nam sản xuất
Tại cuộc họp, sau khi nghe báo cáo của các tiểu ban chuyên môn thẩm định hồ sơ và Kết luận của Hội đồng Đạo đức tại ngày 22-8, các thành viên Hội đồng tư vấn cấp Giấy đăng ký lưu hành thuốc và nguyên liệu làm thuốc (Hội đồng tư vấn) đã thảo luận và xem xét kỹ lưỡng các nội dung liên quan của hồ sơ đăng ký vắc-xin trên.
Tất cả các thành viên Hội đồng tư vấn đã thống nhất kết luận như sau:
Bộ phận thường trực Hội đồng tư vấn và các đơn vị liên quan đã rất khẩn trương, sát sao hướng dẫn doanh nghiệp hoàn thiện hồ sơ trong thời gian sớm nhất theo đúng tinh thần cấp bách và quy trình cuốn chiếu. Hội đồng tư vấn đã nghiên cứu rất kỹ và xem xét một cách cẩn trọng hồ sơ. Hồ sơ đã được Tiểu ban Pháp chế thẩm định 2 lần, Tiểu ban Chất lượng thẩm định 4 lần, Tiểu ban Dược lý, Lâm sàng thẩm định 3 lần.
Các ý kiến thẩm định của các tiểu ban chuyên môn đối với hồ sơ pháp lý, chất lượng, dược lý, lâm sàng và kết luận của Hội đồng Đạo đức trong nghiên cứu y sinh học Quốc gia (Hội đồng Đạo đức) là cơ sở để Hội đồng tư vấn thảo luận, xem xét việc cấp giấy đăng ký lưu hành vắc-xin Nano Covax theo quy định tại Nghị quyết số 86/NQ-CP ngày 6-8-2021 của Chính phủ và Thông tư số 11/2021/TT-BYT ngày 19-8-2021 của Bộ Y tế.
Sau buổi họp, Hội đồng tư vấn ghi nhận các kết quả đạt được đối với hồ sơ đề nghị cấp giấy đăng ký lưu hành của vắc-xin Nano Covax đã được các tiểu ban chuyên môn thẩm định, Hội đồng Đạo đức nghiệm thu. Đồng thời, Hội đồng tư vấn đề nghị doanh nghiệp tiếp tục bổ sung, làm rõ các nội dung sau:
Theo đó, về hồ sơ chất lượng: Căn cứ kết quả thẩm định của tiểu ban chất lượng, đề nghị doanh nghiệp bổ sung, cập nhật một số nội dung theo ý kiến của tiểu ban chất lượng theo hình thức cuốn chiếu.
Về hồ sơ dược lý, lâm sàng: Căn cứ kết quả thẩm định hồ sơ lâm sàng của Trung tâm Dược lý lâm sàng – Trường Đại học Y Hà Nội và Kết luận của Hội đồng Đạo đức tại Biên bản số 56/BB-HĐĐĐ ngày 22-8, Hội đồng tư vấn đề nghị:

Tiêm vắc-xin Nano Covax cho người tình nguyện
Về tính sinh miễn dịch: Bổ sung, cập nhật dữ liệu theo đề cương sửa đổi mới nhất được Hội đồng đạo đức thông qua, bao gồm: Bổ sung, cập nhật đánh giá tính sinh miễn dịch trên các biến chủng mới (ví dụ biến chủng Delta, biến chủng Anh…) và cỡ mẫu đánh giá tính sinh miễn dịch cần thực hiện theo đúng đề cương nghiên cứu đã được thông qua.
Về hiệu quả bảo vệ: Đề nghị doanh nghiệp phối hợp với nhóm nghiên cứu để phân tích, bàn luận về mối liên quan giữa tính sinh miễn dịch của vắc-xin và hiệu quả bảo vệ tối thiểu 50% (theo hướng dẫn của Tổ chức Y tế thế giới – WHO) dựa trên các dữ liệu y văn.
Các thành viên hội đồng cũng đề nghị doanh nghiệp khẩn trương bổ sung, cập nhật các nội dung nêu trên, báo cáo Hội đồng Đạo đức và Hội đồng tư vấn tiếp tục xem xét, thẩm định cuốn chiếu các kết quả nghiên cứu để có thể cấp giấy đăng ký lưu hành có điều kiện trong trường hợp cấp bách.
Đến thời điểm hiện tại, Nano Covax là vắc-xin Covid-19 đầu tiên của Việt Nam đang thử nghiệm lâm sàng giai đoạn thứ 3. Sau hơn 8 tháng tiến hành 3 giai đoạn thử nghiệm lâm sàng vắc-xin Nano Covax, đã có gần 14.000 người được tiêm thử nghiệm.
Theo khuyến cáo của Tổ chức Y tế thế giới, hiệu quả bảo vệ của vắc-xin nếu đạt trên 50% có thể được xét cấp phép khẩn cấp.
Lãnh đạo Bộ Y tế cho biết việc cấp phép cần dựa trên những bằng chứng khách quan, minh bạch, khoa học được Hội đồng Đạo đức và Hội đồng tư vấn cấp giấy đăng ký lưu hành thuốc, nguyên liệu làm thuốc xem xét, đánh giá. Đây là 2 Hội đồng độc lập và Bộ Y tế sẽ xem xét việc cấp phép đối với một thuốc, vắc-xin khi thuốc, vắc-xin đó được 2 Hội đồng thông qua.
Vắc-xin là sản phẩm đặc biệt, vì vậy cần xem xét cẩn thận, kỹ lưỡng, đặc biệt có sự tham vấn của các nhà khoa học uy tín, các tổ chức quốc tế… và có những bước đi cẩn trọng từng bước để có thể đánh giá về tính an toàn (ngắn hạn và dài hạn), sự ổn định và sự bền vững của tính sinh miễn dịch, đặc biệt là hiệu quả bảo vệ.
Nguồn NLĐ

































0 Bình luận
Hãy là người đầu tiên gửi bình luận.